3D принтеры способны не только лишь создавать 6-секундные зубные щетки и цифровые камеры, сейчас они могут также создавать микроскопичные бактериальные «клетки».

Этот трехмерный череп шимпанзе был написан с той же основной технологией, которую на данный момент употребляют в лаборатории Шира для печати бактериальных клеток. Фото: Джейсон Шир
Замыкая бактерии в микроскопичных домиках, ученые Техасского института в Остине изучают, как болезнетворные бактерии, такие как отысканные в кишечном тракте и легких человека, ведут взаимодействие и развивают инфекции.
В недавнешнем опыте они показали, как колония золотистого стафилококка, способная вызвать некие виды кожной инфекции, стала более устойчивой к лекарствам, когда она находилась снутри огромного общества синегнойной палочки, бактерии, вызывающей разные заболевания, в том числе муковисцидоз. Работу на этой неделе выпустили в Трудах Государственной академии.
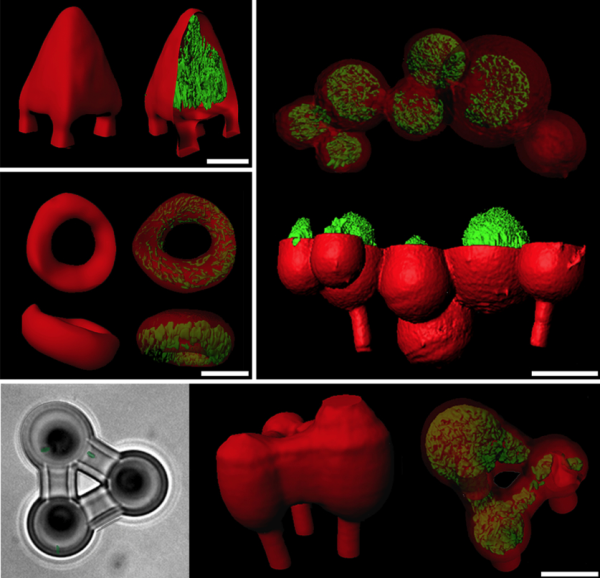
Исследователи употребляют новейшую технологию 3D печати, чтоб выстроить дома для микробов на микроскопичном уровне. Их способ предполагает внедрение лазера для построения белковых «клеток» вокруг микробов в желатине. Приобретенные структуры могут иметь фактически всякую форму либо размер и могут быть перемещены по отношению к другим структурам, содержащим бактериальные микросообщества.
Способ должен позволить проводить полностью новый класс тестов при критериях, более соответственных тем, с которыми бактерии сталкиваются в реальных био средах, таких как человеческое тело.
«Это позволяет нам практически найти каждую переменную», – гласит Джоди Коннел, постдокторский исследователь в институте естественных наук.
«Мы можем найти пространственные особенности в масштабах, соответственных тем, что ощущает и чувствует одна амеба. Мы также можем еще поточнее имитировать виды сложных бактериальных экологий, которые есть в реальных инфекциях, когда в их находится не один вид, а ведет взаимодействие сходу несколько разных видов бактерий».
В базе данного способа лежит желатиновый реагент, который имеет несколько главных особенностей. Бактерии могут в нем комфортно жить и плодиться. В тепле этот раствор становится водянистым, но при комнатной температуре он становится желеподобным. Находящиеся в нем светочувствительные молекулы принуждают желатиновые молекулы вступать в реакцию и соединяться вместе под воздействием света.
Бактерии помещают в раствор. Когда он охлаждается, бактерии застывают на месте. Коннел и ее коллеги, включая Джейсона Шира, доктора химии, и Марвина Вайтели, доктора молекулярных био наук, определяют, какие бактерии они желают поместить в клеточку и в какой форме. Потом они зажигают лазер, используя чип, переделанный из кинопроектора, чтоб спроецировать двумерное изображение в желатин. Всюду, где оно фокусируется, формируются твердые матрицы.
«Затем мы делаем очередной слой, и 2-ой, и так далее», – гласит Шир. «Все до боли просто. Мы практически делаем фото и укладываем их в 3D структуры, но весь процесс кропотливо контролируется. Задумайтесь о толщине волоска на вашей руке, возьмите от этого 1%, а потом еще четверть от этого. Это и будет примерный размер лазера».
После того, как структура завершена, микробам можно ввести питательные вещества и позволить воспроизводиться в ограниченном пространстве до контролируемой плотности. Ученые могут взять другие микросообщества в клеточках и расположить их довольно близко друг от друга, чтоб колонии вели взаимодействие вместе. Можно даже смыть избытки желатина, приостановить рост микробов и сохранить их для предстоящей транспортировки в лаборатории, расположенные в других частях мира.
«Главным будет то, что эти структуры можно не только лишь держать под контролем исходя из убеждений их формы, они также очень био-доброжелательные», — гласит Шир. «Стены, которые мы делаем из этих белковых молекул, связаны вместе довольно плотно, чтоб не позволить микробам освободиться, но они довольн
о пористые, чтоб вступать в хим взаимодействия. Питательные вещества могут проходить. Отходы могут выходить наружу. Может осуществляться обмен сигналами. Они заключены в этих малеханьких домиках, но работают, как обычно в био среде».
Шир заявил, что новенькая техника должна позволить проводить им широкий диапазон тестов. Рост можно остановить на любом шаге, чтоб сделать анализ выраженности генов микробов, поглядеть какие гены врубаются/выключаются в ответ на изменение критерий. Разные виды микробов можно вынудить вести взаимодействие в разных конфигурациях, при разных плотностях, в разных временных рамках. Бактерии, такие как стафилококк и синегнойная амеба, можно организовать в виде «ядро-оболочка», с ядром в виде стафилококка, окруженного оболочкой синегнойных микробов, чтоб поглядеть, что происходит, когда они сразу сталкиваются с ненужными для их антибиотиками.
«Это вправду самые всераспространенные бактерии, которые нередко встречаются совместно в инфекциях, потому, естественно, они владеют определенными механизмами для чувства друг друга», – гласит Шир. «Эта разработка позволяет нам вынудить их вести взаимодействие, и поглядеть, что произойдет. В данном случае стафилококк ощутил синегнойную бактерию, одним из последствий стало то, что он стал более устойчивым к антибиотикам».
Посреди длительных целей: использовать информацию, полученную в процессе этих тестов, чтоб более отлично биться с человечьими инфекциями.
«Подумайте о поликлинике, это не самое наилучшее место, где реально избежать столкновения с инфекциями», – гласит Шир. «Существуют исследования, которые, похоже, свидетельствуют, что инфекции передаются через очень мелкие микроколонии микробов, которые, вероятнее всего, передаются через инструменты, оборудование и персонал из одной части поликлиники в другую. На этот момент мы не достаточно знаем, о том, как это происходит. Сколько на это уходит клеток? Становятся ли подобные микросообщества небезопасными либо устойчивыми к лекарствам конкретно поэтому, что они мелкие, а потом, в свою очередь, изменяют функции микробов, нашей кожи либо тела? Сейчас мы желаем разглядеть все эти вопросы шире».